- Категория: статии
ЗАХАРЕН ДИАБЕТ
Захарният диабет е най-разпространеното ендокринно заболяване, от което страда около 3% от населението в света.
Това е хронично заболяване, характеризиращо се с повишена кръвна захар, поради нарушено производство на инсулин от задстомашната жлеза и недостатъчната му ефективност.
Инсулинът е хормон, който се отделя от т. нар. бета клетки на панкреаса (задстомашната жлеза), като неговата основна задача е да понижава нивото на кръвната захар до нормалните и стойности (3,5 – 5,5 ммол/л).
Съществуват два типа захарен диабет:
![]() Диабет тип 1 – характеризира се с нарушение в производството на инсулин от панкреаса. Поради това този тип диабет е инсулинозависим. Той засяга 10 - 15% от диабетиците и се появява по-често по време на детството;
Диабет тип 1 – характеризира се с нарушение в производството на инсулин от панкреаса. Поради това този тип диабет е инсулинозависим. Той засяга 10 - 15% от диабетиците и се появява по-често по време на детството;
![]() Диабет тип 2 – характеризира се с нарушена чувствителност на клетките към действието на инсулина (инсулинова резистентност), забавяне или недостиг на секрецията му. Този тип диабет в повечето случаи е инсулинонезависим. Това е по-разпространената форма на диабет, тъй като тя засяга 85 - 90% от диабетиците. След години, с давността на диабета в някои случаи инсулиновите резерви се изчерпват и захарният диабет тип 2 става инсулинозависим.
Диабет тип 2 – характеризира се с нарушена чувствителност на клетките към действието на инсулина (инсулинова резистентност), забавяне или недостиг на секрецията му. Този тип диабет в повечето случаи е инсулинонезависим. Това е по-разпространената форма на диабет, тъй като тя засяга 85 - 90% от диабетиците. След години, с давността на диабета в някои случаи инсулиновите резерви се изчерпват и захарният диабет тип 2 става инсулинозависим.
Храненето при диабетно болните играе важна роля в поддържането на кръвната захар в нормални стойности. Необходимо е да се знае, че препоръките за хранене на диабетно болните не се различават от тези за здравите хора.
Правилният прием на въглехидрати (захари) е от първостепенно значение за нормализиране на кръвната захар. Въглехидратното съдържание на храната се измерва в хлебни единици (ХЕ).
1 хлебна единица = 12 грама въглехидрати.
Диабетно болният трябва да познава храните, съдържащи въглехидрати; да знае от колко ХЕ дневно се нуждае и да разпределя правилно дневните ХЕ в 3 основни и 2 междинни хранения.
Гликемичен индекс (Gl)
Някои въглехидратни храни повишават по-бързо и рязко кръвната глюкоза след хранене в сравнение с други такива. Първата група храни има висок гликемичен индекс, а втората – нисък.
Диабетиците могат успешно да контролират нивото на кръвната си захар, като избират и предпочитат храни с нисък гликемичен индекс (сурови зеленчуци и плодове, варива, спагети, пълнозърнест хляб, овес, нискомаслено мляко).
Примери:
1. Една филийка бял хляб и една филийка пълнозърнест хляб съдържат еднакво количество въглехидрати – по 1 ХЕ, но белият хляб има по-висок гликемичен индекс (по-бързо и рязко повишава кръвната захар след хранене) в сравнение с пълнозърнестия;
2. Половин филийка хляб и една сурова необелена ябълка съдържат едно и също количество въглехидрати – по 1 ХЕ, но ябълката повишава по-бавно и плавно кръвната захар – т. е. има по-нисък гликемичен индекс в сравнение с хляба.
Не се преизчисляват в хлебни единици: нетлъсти меса (говеждо, телешко, свинско филе, заек, пиле без кожата, дивеч); нетлъсти риби (бяла риба, пъстърва, калкан, мерлуза, копърка); сирене (предимно краве); яйца; зеленчуци; чай, кафе (без захар) и минерална вода”.
Други фактори, влияещи върху нивото на кръвната захар са:
• Кулинарната обработка на храните – суровите плодове, печените и леко сварените ястия са с по-нисък гликемичен индекс от естествените плодови сокове или компоти, пържените и преварените храни;
• Комбинирането на храните – приемът на въглехидрати заедно с мазнини и белтъчини забавя постъпването на глюкозата в кръвта;
• Технологичното рафиниране на храните – пълнозърнестото брашно има по-нисък гликемичен индекс от бялото брашно;
• Степента на зрялост на плодовете – леко узрелите плодове имат не само по-малка сладост, но и по-нисък гликемичен индекс в сравнение с презрелите;
• Съдържанието на фибри (целулоза, хемицелулоза, пектин, лигнин, слизести вещества и други) в хранителните продукти – плодовете, зеленчуците, зърнените храни, варивата и пълнозърнестият хляб са богати на фибри и имат нисък гликемичен индекс.
Нашето здраве в болшинството от случаите е в нашите ръце, но при захарния диабет - не е точно така. Учените все още не са разбулили напълно тайната, стояща в основата на това страдание. Знае се, че всеки от нас носи своята наследственост, която за съжаление при диабета е определяща. Тя обаче не е достатъчна, за да станем диабетици. Ние не унаследяваме самото заболяване, а тенденцията за неговата изява. Срещата ни с редица външни фактори като вируси, химикали, стресови ситуации и други могат да отключат поредица от автоимунни процеси в нашия организъм, които да увредят и унищожат клетките на панкреаса, отделящи хормона инсулин. По този начин се развива т. нар. младежки тип диабет. В по-късна възраст, ако увеличим прекомерно теглото си вероятността да се разболеем от диабет нараства многократно.
Ние не можем да променим нашата наследственост, но сме в състояние да променим своя начин на живот. Ако се погрижим за здравето си навреме чрез здравословно хранене, ежедневна двигателна активност и успеем да придобием умения за справяне със стреса, можем сами да намалим вероятността да се разболеем от диабет.
ТРЯБВА ДА СЕ КОНСУЛТИРАМЕ С ЛИЧНИЯ СИ ЛЕКАР:
АКО СМЕ НА ВЪЗРАСТ ДО 40 ГОДИНИ И СЕ ОПЛАКВАМЕ ОТ:
• често уриниране, дори и нощем;
• сухота в устата и приемане на много течности – над 10 чаши дневно;
• повишен апетит, съпроводен със загуба на тегло;
• намалена работоспособност и затруднена умствена концентрация;
• чести кожни инфекции и трудно зарастващи рани;
• замъглено зрение;
• сексуални проблеми и др.
АКО СМЕ НА ВЪЗРАСТ НАД 40 ГОДИНИ И СЕ ОПЛАКВАМЕ ОТ:
• наднормено тегло – обиколката на талията ни е над 1/2 от височината;
• упорит сърбеж и чести възпаления в областта на половите органи;
• гнойни инфекции на кожата;
• гъбични заболявания;
• трудно зарастващи рани;
• сексуални проблеми и др.
АКО КРЪВНАТА НИ ЗАХАР Е:
• над 7,0 ммол/л на гладно
или
• над 11,1 ммол/л 2 часа след нахранване
Когато сме болни от диабет могат да настъпят остри и хронични усложнения.
![]() Към острите се отнасят резките промени в нивото на кръвната захар, които могат да бъдат:
Към острите се отнасят резките промени в нивото на кръвната захар, които могат да бъдат:
ПОНИЖАВАНЕ под 4 ммол/л
Тогава ще почувстваме: безпокойство, главоболие, сърцебиене, изпотяване, тремор, чувство на глад, които могат да прогресират до помрачаване на съзнанието.
Трябва да помним, че това е най-опасното за живота на диабетика състояние. Ето защо е необходимо винаги да носим в себе си захар (напр. 3-4 бучки в кутийка или 3 пакетчета захар за кафе), която да приемем, когато усетим появата на посочените симптоми.
ЗНАЧИТЕЛНО ПОВИШАВАНЕ
Тогава ще почувстваме: гадене, повръщане, повишена жажда, учестено уриниране, обща слабост, коремна болка, зрителни смущения, и замъгляване на съзнанието.
В този случай е необходимо веднага да потърсим лекарска помощ.
![]() Към късните усложнения на диабета се отнасят уврежданията на кръвоносните съдове на очите, бъбреците, крайниците, сърцето и мозъка. С развитието на болестта може да почувстваме: намаление на зрението; главоболие; изтръпване на долните крайници; изстиване на краката; намаление на мускулната сила; болки в сърдечната област и други. Тези оплаквания алармират, че късните усложнения в нашия организъм вече са настъпили. Ето защо е необходимо да вземем мерки преди това - стриктно да изпълняваме съветите на своя лекар и ежегодно да се консултираме със специалист.
Към късните усложнения на диабета се отнасят уврежданията на кръвоносните съдове на очите, бъбреците, крайниците, сърцето и мозъка. С развитието на болестта може да почувстваме: намаление на зрението; главоболие; изтръпване на долните крайници; изстиване на краката; намаление на мускулната сила; болки в сърдечната област и други. Тези оплаквания алармират, че късните усложнения в нашия организъм вече са настъпили. Ето защо е необходимо да вземем мерки преди това - стриктно да изпълняваме съветите на своя лекар и ежегодно да се консултираме със специалист.
ЗА ДА ПРОДЪЛЖИМ ДА ЖИВЕЕМ ПЪЛНОЦЕННО Е НЕОБХОДИМО......
![]() да спазваме предписаното ни медикаментозно лечение;
да спазваме предписаното ни медикаментозно лечение;
![]() да се храним здравословно като:
да се храним здравословно като:
• изключим захарта и захарните изделия от ежедневното си меню;
• разпределим храната в 3 основни и 2-3 междинни приема, като спазваме часовете за хранене;
• намалим консумацията на мазнини и особено на животинските, които съдържат холестерол;
• ограничим консумацията на месо и почти изключим колбасите от менюто си;
• консумираме нетлъсти меса в количества 50-100 г дневно, 2-4 пъти седмично;
• използваме варене, печене и задушаване на ястията без допълнителна мазнина;
• консумираме млека с ниска масленост – до 2%;
• консумираме хляб и тестени изделия от пълнозърнести брашна;
• консумираме 2-3 пъти седмично варива, картофи и ориз за сметка на хляба от съответното хранене;
• консумираме сурови и готвени зеленчуци няколко пъти дневно;
• консумираме 2-3 плода дневно или 1-2 шепи малини, къпини, ягоди, боровинки;
• ограничим консумацията на готварска сол;
• внимаваме с т. нар. храни за диабетици, които не могат да се консумират без ограничения и често са богати на скрити мазнини и захари;
• използваме за подслаждане заместители на захарта;
• ограничим консумацията на алкохол и не го приемаме “на гладно”;
• прекратим тютюнопушенето;
• пием 1,5 л вода дневно, ако лекарят не е назначил друго.
![]() да упражняваме физическа активност ежедневно – гимнастика, разходки, туризъм и други.
да упражняваме физическа активност ежедневно – гимнастика, разходки, туризъм и други.
- Категория: статии
Затлъстяване
Затлъстяването е заболяване, което се дължи на прекомерно натрупване на мастна тъкан в организма на човека. В зависимост от степента на това натрупване, състоянието се определя като наднормено тегло или като затлъстяване. Затлъстяването е резултат на нарушен енергиен баланс – сътношението между енергийната стойност на храната и енергоразхода на човека – т. е. хората наддават на тегло, когато поемат повече калории, отколкото изгарят. Излишните калории се складират в тялото под формата на тлъстини. Затлъстелите хора носят на гърба си огромно количество излишни мазнини и рисковете за тяхното здраве са сериозни. Затлъстяването е не само естетичен, но и здравословен проблем! То е причина за развитието на редица заболявания: сърдечно-съдови (атеросклероза, артериална хипертония, исхемична болест на сърцето, мозъчен инсулт), захарен диабет тип 2, злокачествени новообразувания, подагра, ставни и дихателни заболявания, и други. В резултат на всичко това затлъстяването съкращава живота и води до преждевременна смърт.
Причини и рискови фактори
За развитието на заболяването играят роля няколко различни групи фактори:
Генетични фактори. При наличие на един родител със затлъстяване вероятността детето да развие затлъстяване достига 40%, при двама родители вероятността достига 80%. Без фамилна обремененост този процент е 10.
Фактори на средата. В много случаи средата на живот не благоприятства здравословния начин на живот. Примери за това са липсата на достъпни съоръжения за спорт, паркове и велосипедни алеи; големите размери на порциите; състава на храната и др.
Физиологични фактори. В тази група фактори са нарушенията в обмяната на мастната тъкан, хормонални промени и др.
Психологически фактори: При някои хора емоционалното състояние оказва влияние върху храненето. В тази група фактори се включват хранителните разстройства.
Състояния и заболявания като инсулинова резистентност, хипотиреоидизъм, синдром на Кушинг и др.
Медикаменти. Приемът на някои медикаменти се свързва с увеличение на телесната маса: антидепресанти, антиконвулсанти, някои медикаменти, използвани в лечението на диабет, някои хормонални препарати, кортикостероиди и др.
Видове затлъстяване:
В зависимост от разпределението на подкожната мастна тъкан се различават три типа на затлъстяване:
· генерализирано - дебелината на подкожната мастна тъкан нараства по цялото тяло;
· женски тип (гиноидно) или периферно - отлагането на мазнините е предимно в долната част на тялото/ханша/; тялото придобива форма на круша;
· мъжки тип (андроидно) или централно - най-голямо количество мастна тъкан е отложена по корема и гърдите; тялото придобива форма на ябълка.
КАК МОЖЕ ДА ОЦЕНИТЕ ТЕЛЕСНОТО СИ ТЕГЛО?
• Чрез Индекса на телесната маса (ИТМ), който се определя като се раздели теглото в килограми на ръста в метри, повдигнат на квадрат.
Класификация на наднорменото тегло в зависимост от ИТМ
|
Класификация
|
ИТМ (кг/м2)
|
Здравен риск
|
| нормално тегло | 18.5 - 24.9 | нисък |
| наднормено тегло | 25 - 29.9 | леко повишен |
| затлъстяване | >=30 | |
|
30.0 - 34.9 | умерено висок |
|
35.0 - 39.9 | висок |
- трета степен |
> 40 | много висок |
• Чрез измерване на обиколката на талията, която нормално не трябва да надхвърля 94 см при мъжете и 80 см при жените. Обиколка на талията при мъжете над 102 см и над 92 см при жените говори за значително повишен здравен риск от заболявания на сърдечно-съдовата система (инфаркт на миокарда, мозъчен инсулт). Установено е, че с нарастването на обиколката на талията се увеличава и кръвното налягане.
• Чрез измерване на съотношението талия/ханш, което дава представа за разпределението на телесните мазнини. Нормално съотношението талия/ханш трябва да е по-малко от 1,0 за мъжете и от 0,85 за жените. Доказано е, че честотата на сърдечно-съдовите и мозъчно-съдовите инциденти расте с повишаване на съотношението талия/ханш и при двата пола.
За определяне на теглото и телесния състав в съвременната медицина се използват и професионални анализатори, които дават информация за ИТМ, процентното съдържание на мазнините в организма, мускулната маса, общото количество вода и други.
Методи за лечение
Съществуват различни методи за лечение: диетолечение, двигателна активност, поведенческа терапия; лечение с медикаменти, хирургични методи и др.
Тъй като затлъстяването е резултат от нарушен енергиен баланс – повишен енергиен внос и/или намален енергиен разход, основните принципи на лечение включват тези два аспекта.
Намаляване на енергийния внос може да се постигне чрез: гладуване; нискокалоричен режим; диети със специален засищащ режим; промяна на хранителното поведение; психологически методи на въздействие – лечение на стреса, социална подкрепа и др.; средства, потискащи апетита.
Всяко лечение е индивидуално и е под наблюдение на специалист диетолог.
КАК МОЖЕ ДА ИЗБЕГНЕТЕ ЗАТЛЪСТЯВАНЕТО?
Като промените хранителните и двигателните си навици, макар това да не е никак лесно.
За да поддържате здравословно телесно тегло, спазвайте следните правила:
• Приемайте храна с енергийна стойност, съответстваща на Вашия енергоразход. Съвременният човек в активна трудова възраст (30 – 60 години) упражнява ниска или умерена физическа активност, поради което средната енергийна потребност за мъжете е съответно 2583 ккал/ден и 2927 ккал/ден, а за жените - съответно 1988 ккал/ден и 2252 ккал/ден.
• Хранете се често и умерено (разпределете храната в 3 основни приема с 2-3 междинни закуски и намалете обема на порциите);
• Спазвайте определени часове на хранене; вечеряйте не по-късно от 2-3 часа преди лягане;
• Увеличете консумацията на плодове и зеленчуци; редовно консумирайте варива и зърнени храни. Тези продукти са бедни на мазнини и богати на хранителни влакнини, които увеличават обема на храната и засилват усещането за ситост;
• Избягвайте пикантните подправки и солта;
• Пийте най-малко 1,5 л вода и течности дневно;
• Намалете консумацията на мазнини и алкохол, тъй като те са висококалорични;
• Ограничете консумацията на сладкарски и тестени изделия (пасти, торти, шоколадови десерти, баници и други), тъй като освен въглехидрати те съдържат и голямо количество мазнини;
• Движете се ежедневно, като ходите пеша или упражнявате леки физически упражнения.
МЕТАБОЛИТЕН СИНДРОМ
Още през 1940 година за пръв път се предполага, че обменните нарушения са предпоставка за възникване и на сърдечно-съдови заболявания. Тази връзка вече е доказана и е дефинирана като заболяване, наречено метаболитен синдром. Заболяването е известно още като синдром Х или дисметаболитен синдром.
Метаболитният синдром е едно от най-често срещаните заболявания на обменните процеси. Последните проучвания на Световната Здравна Организация (СЗО) са изключително тревожни, тъй като доказват, че всеки четвърти човек, т.е. 25% от населението, страда от тази болест. С възрастта възможността за развитието на метаболитен синдром у отделния индивид тенденциозно се увеличава.
Синдромът представлява съвкупност от обменни нарушения, които при едновременна изява, увеличават многократно (до 30 пъти) риска от развитие на сърдечно-съдови заболявания, диабет и онкологични заболявания, които са „бичът” на 21 век.
Метаболитният синдром включва:
1. наднормена обиколка на талията;
2. високо кръвно налягане (хипертония);
3. повишен общ холестерол или нисък HDL (т.н. „добър” холестерол);
4. повишени триглицериди;
5. повишена кръвна захар на гладно или инсулинова резистентност.
За поставянето на диагнозата „Метаболитен синдром” е необходимо определянето на: обиколка на талията, индекс на телесно тегло, количество подкожни мазнини, биохимични кръвни показатели. Особено показателна е обиколката на талията.
Съгласно критериите на СЗО при наличието на затлъстяване, съпътствано дори от два от останалите показатели (нарушен глюкозен толеранс, нарушена кръвна захар на гладно, инсулинова резистентност, хипертония, високи стойности на холестерол или триглицериди) може да се постави диагнозата „Метаболитен синдром”.
Точният механизъм на развитие на метаболитния синдром не е напълно изяснен, но е доказано, че затлъстяването в горните отдели на тялото и особено в коремната област, предразполага към диабет, атеросклероза, подагра и камъни в бъбреците и жлъчката. Към основните рискови фактори за Метаболитния синдром се отнасят: наднорменото тегло, фамилната обремененост, хормоналните нарушения (напр. синдромът на поликистозните яйчници при жените), липсата на физическа активност, злоупотребата с алкохол, тютюнопушенето, приема на храни, съдържащи голямо количество мазнини и въглехидрати.
С подходяща промени в начина на живот (хранене, физическа активност, редуциране на телесното тегло), разпространението на синдрома може да бъде ограничено.
Основните стратегии за предотвратяване на развитието на метаболитния синдром включват:
![]() Повишена физическа активност (напр. ходене пеша 30 минути всеки ден) и формиране на навици за упражняване на спорт и физическа активност;
Повишена физическа активност (напр. ходене пеша 30 минути всеки ден) и формиране на навици за упражняване на спорт и физическа активност;
![]() Здравословна и нискокалорична диета, изграждане на здравословни хранителни навици при малките деца; контрол от страна на родителите върху хранителния режим на подрастващите;
Здравословна и нискокалорична диета, изграждане на здравословни хранителни навици при малките деца; контрол от страна на родителите върху хранителния режим на подрастващите;
![]() Здравословен начин на живот от най-ранна детска възраст
Здравословен начин на живот от най-ранна детска възраст
- Категория: статии
Тиреотоксикоза, хипертиреоидизъм, Базедова болест
Щитовидната жлеза е най-голямата ендокринна жлеза в човешкото тяло.
Тя се състои от дяла (лоба), свързан помежду си с провлак (истмус).
Хормоните на щитовидната жлеза имат голямо значение за нормалната функция на клетките.
Ако са в излишък, те ускоряват метаболизма и засилват ефекта на симпатиковата нервна система, което води активиране на различни системи на тялото и поява на симптоми, наподобяващи тези при високи нива на адреналин — сърцебиене, тремор, тревожност и други.
Терминът „тиреотоксикоза“ се отнася до клиничен синдром, характеризиращ се повишени серумни нива на щитовидните хормони, по-конкретно тироксин (Т4) и/или трийодтиронин (Т3), независимо от причината.
Хипертиреоидизмът е вид тиреотоксикоза, която се дължи на прекомерното производство и секреция на тиреоидни хормони от щитовидната жлеза.
Разграничаването на тиреотоксикозата, причинена от хипертиреоидизъм, и тиреотоксикоза, която не е причинена от хипертиреодизъм, е от голямо значение, защото лечението е различно.
Тиреотоксикоза:
Според Американската тиреоидна асоциация (American Thyroid Association, ATA) тиреотоксикоза може да възникне в следните случаи:
- при прекомерно стимулиране на щитовидната жлеза от хормонални фактори;
- при непрекъснато активиране на синтезата и секрецията на хормоните на щитовидната жлеза, което води до автономно освобождаване на голямо количество щитовидни хормони;
- при пасивно освобождаване на прекомерни количества хормони на щитовидната жлеза, в резултат на различни автоимунни, инфекциозни, химични или механични състояния;
- ако е налице експозиция на екстратиреоидни (невключващи щитовидната жлеза) източници на щитовидни хормони, които могат да бъдат или ендогенни (овариален тератом (струма оварии); метастатичен диференциран карцином на щитовидната жлеза) или екзогенни (thyrotoxicosis factitia);
Най-честите причини за тиреотоксикоза имат различни патофизиологични особености и включват автоимунни заболявания, функциониращи тиреоидни аденоми и инфекции.
Автоимунните заболявания, водещи до тиреотоксикоза, включват:
- Базедова болест (най-честата причина за хипертиреоидизъм);
- лимфоцитен тиреоидит с хипертиреоидизъм (тоест „тих“ тиреоидит);
- постпартална /следродилна/ тиреотоксикоза;
Неоплазмите, водещи до тиреотоксикоза, включват:
- автономно функциониращи токсични нодули (възли);
- токсична полинодозна (многовъзлеста) гуша;
Инфекциите, които могат да предизвикат тиреотоксикоза, включват:
- подостър тиреоидит;
- в много редки случаи — остър гноен тиреоидит;
Диагнозата на тиреотоксикоза се основава предимно на лабораторни изследвания, включително повишени стойности на свободен Т3 (FT3) и свободен Т4 (FT4), както и на ниски нива на тиреостимулиращ хормон (TSH).
Ако от физикалното изследване се установи нормална или дифузно увеличена щитовидна жлеза (гуша), най-вероятната диагноза е Базедова болест.
Ако се палпират (опипват) един или повече възли на щитовидната жлеза, най-вероятно се касае за автономно функциониращ възел или токсична полинодозна (многовъзлеста) гуша.
Ако щитовидната жлеза е болезнена при палпация, вероятно причината е подостър тиреоидит.
Радиоизотопното изследване на щитовидната жлеза (сцинтиграфия) може да спомогне за разграничаване на Базедова болест от токсичен възел и токсична полинодозна гуша.
Сцинтиграфското изследване за определяне на поглъщането на радиоактивен йод (radioactive iodine uptake, RAIU, радиойодкаптация), сцинтиграфията на щитовидната жлеза и ултразвуково изследване (ехография) на щитовидната жлеза не са основните начини за диагностициране на тиреотоксикоза, но резултатите от тези изследвания могат да спомогнат за поставяне на диагноза, както и при избора на лечение.
Ултразвуково изследване на щитовидната жлеза с цветен Доплер за оценка на кръвоснабдяването на жлезата е ценен тест, спомагащ за разграничаване на деструктивен тиреоидит от Базедова болест, и е особено полезен в случаите, в които използването на радиоактивен йод е противопоказано — например при бременност и кърмене.
Хипертиреоидизъм:
Всички заболявания на щитовидната жлеза се срещат по-често при жените, отколкото при мъжете.
Съотношението мъже-жени при болестта на Базедов 1:5-10, а съотношението мъже:жени за токсична полинодозна гуша и токсичен аденом е 1:2-4.
Офталмопатия (всяко заболяване на окото) при болни с базедова болест се наблюдава по-често при жени, отколкото при мъже.
Автоимунните заболявания на щитовидната жлеза са с най-висока честота при хора на възраст 20-40 години.
Токсичната полинодозна струма (гуша) се развива при пациенти, при които обикновено е налице продължителна анамнеза за нетоксична гуша, поради което това състояние обикновено се наблюдава след 50-годишна възраст. При пациентите с токсичен аденом заболяването се развива в по-млада възраст.
Има няколко причини за развитие на хиперитреоидизъм:
В повечето от случаи цялата жлеза произвежда допълнително щитовидни хормони. В по-редки случаи е налице единичен възел (наречен „горещ“ възел), който е отговорен за излишната хормонална секреция.
Тиреоидитът (възпаление на щитовидната жлеза) също може да причини хипертиреоидизъм.
Основните причини за хипертиреоидизъм включват:
- Базедова болест (позната и като болест на Грейвс) — автоимунно заболяване, което е най-честата причина за хипертиреоидизъм (50-60% от случаите).
Среща се 8 пъти по-често при жени, отколкото при мъже.
Нивата на щитовидните хормони могат да бъдат силно повишени при болестта на Базедов. - Подостър тиреоидит — това е втората по честота причина за тиреоидит (в около 15-20% от случаите), като се характеризира с деструкция (разрушаване на жлезна тъкан) и последващо освобождаване на прекурсорен протеин;
- Токсичен аденом на щитовидната жлеза — съставлява около 3-5% от случаите с тиреотоксикоза. Токсичният аденом представлява хиперфункциониращ единичен възел.
Токсична полинодозна гуша (болест на Plummer)— съставлява 10-15% от случаите на тиреотоксикоза. Наблюдава се по-често при възрастни индивиди, особено при пациенти с дългогодишна анамнеза за гуша.
Симптомите на тиреотоксикоза са по-слабо изразени, защото е налице само леко повишение на нивата на щитовидните хормони.
При това състояние обаче нивата на щитовидните хормони могат значително да се увеличат след прием на голямо количество йод (например при изследване с йод-съдържащи контрастни средства или при прием на амиодарон).
Високите нива на щитовидни хормони в кръвта (най-точен термин е хипертироксинемия) могат да се дължат и на други, по-рядко срещани причини, включително:
Тиреоидит — възпаление на щитовидната жлеза. Има няколко различни вида тиреоидит, включително тиреоидит на Хашимото и подостър тиреоидит (на de Quervain). Тези състояния водят до хормонален дефицит и хипотиреоидизъм, но в началните етапи може да е налице свръхсекреция на тиреоидни хормони;
Предозиране с хормони на щитовидната жлеза при назначена хормонозаместителна терапия;
Прием на амиодарон — антиаритмичен препарат, който е структурно подобен на тироксин (Т4) и може да доведе до повишена активност на щитовидната жлеза;
Постпартален (следродилен) тиреоидит — наблюдава се при около 7% от жените през първата година след раждането.
Постпарталният тиреоидит има няколко фази, първата от които е хипертиреоидизъм.
Овариален тератом (струма оварии) — това е рядко срещана форма на тератом, който съдържа предимно тироидна тъкан, която може да секретира прекомерни количества тиреоидни хормони — хипертиреоидизъм;
При пациентки с гроздовидна бременност (mola hydatidosa) или хориокарцином се установяват изключително високи нива бета-човешки хорионгонадотропин (β-hCG), което може да доведе до активиране на рецепторите за тиреостимулиращ хормон (TSH), което е достатъчно да причини тиреотоксикоза;
Метастатичен фоликуларен тиреоиден карцином — при тези новообразувания е запазено производството на хормони на щитовидната жлеза, като при пациенти с по-големи по размер тумори производството може да бъде достатъчно високо, за да доведе до тиреотоксикоза;
Прекомерен прием на йод (феномен на йод-Базедов) — например при пациенти, които се изследват с йод-контрастни вещества, или такива, които консумират храна, богата на йод.В повечето случаи, след изчерпване на излишното количество йод, функцията на щитовидната жлеза се нормализира.
Има няколко генетични синдроми, които са асоциирани с хипертиреоидизъм, особено автоимунните заболявания на щитовидната жлеза.Синдромът на McCune-Albright възниква в резултат от мутации в GNAS гена, като един от симптомите му е хипертиреоидизъм.
Клиничните прояви при пациентите с хипертиреоидизъм са разнообразни. Проявите на хипертиреоидизъм обикновено започват бавно, но при някои млади пациенти тези прояви могат да бъдат внезапни. В началото симптоми могат да бъдат объркани с нервност, причинена от стрес.
По-често срещаните симптоми и признаци на хипертиреоидизъм включват:
- нервност;
- раздразнителност;
- безпокойство;
- повишено изпотяване;
- непоносимост към топлина;
- хиперактивност;
- сърцебиене;
- тахикардия или предсърдна аритмия;
- топла, влажна, гладка кожа;
- втренчен поглед;
- тремор (треперене) на ръцете;
- загуба на тегло въпреки повишения апетит;
- менструални нарушения;
- нарушения на съня;
- мускулна слабост;
Паник атаки, нарушена концентрация и проблеми с паметта също могат да възникнат.
Също така може да се наблюдава засилена чревна перисталтика, като диарията е често срещан симптом. Може също така да има гадене и повръщане.
При голяма част от пациентите се наблюдава пълна ремисия на симптомите 1-2 месеца след достигане на еутиреоидно състояние (нормална функция на щитовидната жлеза), като това се изразява с намаляване на тревожността, чувството на изтощение, раздразнителността и депресията.
Някои пациенти може да се оплакват от повишено безпокойство или състояние на афективни и когнитивни симптоми в продължение на десет години.
При субклиничен хипертиреоидизъм (характеризира се с ниски нива на тиреостимулиращ хормон (ТСХ) и с нормални нива на щитовидните хормони — FT3 и FT4) са налице слабо изразени (ако въобще има) симптоми на тиреотоксикоза.
Честотата на субклиничния хипертиреоидизъм може да достигне 2% от общата популация.
- Физикалното изследване също има голямо значение в поставянето на диагноза.
При болест на Базедов щитовидната жлеза е дифузно уголемена и уплътнена.
При токсичната полинодозна (многовъзлеста) гуша щитовидната жлеза е 2 до 3 пъти по-голяма от нормалния си размер. Жлезата обикновено е с мека консистенция, като в някои случаи могат да бъдат палпирани (опипани) отделни възли. Тъй като повечето нодули (възли) на щитовидната жлеза не могат да бъдат палпирани, необходимо е да се направи ултразвуково изследване на щитовидната жлеза.
Свръхактивните (горещи) възли на жлезата обаче могат да бъдат диагностициране само чрез сцинтиграфия на щитовидната жлеза с радиоактивния изотоп технеций 99m (Tc99m) или йод-123 (I-123).
Ако щитовидната жлеза е уголемена и болезнена, най-вероятната диагноза е болезнен подостър грануломатозен тиреоидит. Трябва да се обмисли и дегенерация или кръвоизлив на възел, както и гноен тиреоидит.
При около 50% от пациентите с базедова болест е налице лека тиреоид-асоциирана офталмопатия. Обикновено офталмопатията се проявява само като периорбитален оток (оток на тъканите около очите), но може да включва и: - конюнктивален оток (хемоза);
- инекция (зачервяване на видимата част на окото);
- незатваряне на клепачите;
- изоставане на горния клепач при поглед надолу (признак на Грефе/Graefe);
- екстраокуларна мускулна дисфункция (диплопия);
- проптоза (изпъкване на очната ябълка);
Тези очни симптоми обаче не трябва да се бъркат с екзофталма, който е специфичен за хипертиреоидизъм, причинен от болестта на Базедов (не всеки екзофталм се дължи на това заболяване, но когато екзофталмът е придружен от хипертиреоидизъм — това е патогномоничен белег за базедова болест). Изпъкването на очните ябълки се дължи на имуномедиирано възпаление на ретроорбиталната (намираща се зад очната ябълка) мастна тъкан.
В редки случаи болестта на Грейвс засяга кожата чрез отлагане на гликозаминогликани в дермата на подбедрицата. Това води до оток, който обикновено е придружен от задебеляване на кожата, без обаче да е налице болка или пруритус.
Тиреотоксичната криза (известна и като тиреоидна буря) е тежка форма на тиреотоксикоза, характеризираща се с: бърз и често неравномерен сърдечен ритъм; висока температура;
повръщане; диария; напрежение; безпокойство;
Тиреоидната буря е спешно състояние, което изисква незабавна медицинска помощ. Дори при адекватно лечение, смъртността достига 20-50%.
Диагностицирането на хипертиреоидизъм включва различни методи:
Лабораторни изследвания.
Основното изследване за диагностициране на промените във функцията на щитовидната жлеза е изследването на тиреостимулиращия хормон (TSH, ТСХ).
При тиреотоксикоза нивата на TSH обикновено са много ниски (< 0.05 mU/mL).
Въпреки че изследването на TSH е най-надеждният метод за оценка на функцията на щитовидната жлеза, тежестта на хипертиреоидизма не може да се определи чрез този тест — необходимо да се изследват нивата на щитовидните хормони. Тежестта на клиничните прояви много често не корелира със степента на повишаване на нивата на щитовидните хормони.
Щитовидните хормони са трийодтиронин (Т3) и тироксин (Т4), като над 99% от хормоните са свързани със серумни протеини (тироксин-свързващ глобулин, транстиретин и албумин). При пациенти със съмнение за хипертиреоидизъм (когато стойностите на TSH ниски) се препоръчва изследване на свободен Т4 (FT4) и общ Т3.
Изявеният първичен хипертиреоидизъм се характеризира с нива на ТСХ под референтните граници и повишени нива на щитовидните хормони.
Субклиничният хипертиреоидизъм е по-лека форма на хипертиреоидизъм, която се характеризира с ниски нива на TSH, но нормални стойности на Т3 и Т4.При индивидите със субклиничен хипертиреоидизъм е налице повишен риск (42%) от костни фрактури.
Хормоналните промени при бременност могат да затруднят интерпретирането на резултатите от тестовете за изследване на функцията на щитовидната жлеза. Физиологичното повишаване на нивата на бета-човешкия хорионгонадотропин (β-hCG) в края на първия триместър на бременността е свързано с временно понижаване на ТСХ. Въпреки че нивата на TSH се понижават, нивата на FT4 обикновено остават нормални или са малко над референтните граници. С напредване на бременността нивата на TSH се нормализират.
Изследване за антитела:
За диагностициране на автоимунен тиреоидит е необходимо да се направи тест за антитела, като най-специфичното изследване е ELISA тест за антитела срещу тиреоидната пероксидаза (анти-ТРО).
Титрите обикновено са значително повишени при най-често срещаната причина за хипертиреоидизъм — болест на Грейвс, а при токсична полинодозна гуша и токсичен аденом титрите обикновено са ниски.
При голям брой здрави хора без активна болест на щитовидната жлеза обаче се установяват леко повишени титри за анти-TPO, поради което това изследване не трябва да се използва за скрининг.
Ако причината за тиреотоксикоза все още не е изяснена след физикалния преглед и лабораторните изследване, тя може да бъде потвърдена чрез сцинтиграфия.
Класификацията на възлите на щитовидната жлеза като „студени“, „топли“ или „горещи“ се определя от тяхната способност да натрупват радиоактивно вещество спрямо околния нормален паренхим:
студен възел — не се натрупва радиоактивно вещество;
топъл възел — натрупва се по-голямо количество радиоизотоп в сравнение с други участъци на жлезата;
горещ възел — интензивно натрупване на радиоактивно вещество, докато в останалата част на жлезата се натрупва слабо или въобще не се натрупва;
Други изследвания:
При по-възрастни пациенти с хипертиреоидизъм е увеличен рискът от предсърдни аритмии или сърдечна недостатъчност.Ето защо се препоръчва електрокардиограма (ЕКГ), ако се установи:
ускорена сърдечна дейност (> 100 удара/мин);
неправилна сърдечна дейност;
признаци на сърдечна недостатъчност;
Лечението на хипертиреоидизъм включва:
Диета;
Облекчаване на симптомите;
Терапия с антитиреоидни средства;
Терапия с радиоактивен йод-131 (I 131);
Тироидектомия (оперативно отстраняване на щитовидната жлеза);
Нелекуването на хипертиреоидизъм може да доведе до остеопороза.
— Диета:
Не е необходимо пациентите с хипертиреоидизъм да спазват специална диета. Приемът обаче на някои експекторанти, радиоконтрастни вещества, водорасли и хранителни добавки, съдържащи прекомерни количества йод, трябва да се избягват, тъй като йодът пречи на или усложнява лечението с антитиреоидни и радиоактивни препарати.
— Облекчаване на симптомите:
Голяма част от неврологичните и сърдечно-съдовите симптоми при тиреотоксикоза/хипертиреоидизъм — например сърцебиене, треперене и безпокойство — се облекчават чрез терапия с бета-блокери.
Бета-блокерите, които обикновено се използват за лечение на високо кръвно налягане, водят до незабавно временно облекчаване на симптомите при пациенти, страдащи от хипертиреоидизъм, докато се започне продължително лечение на заболяването. Тези медикаменти не лекуват хипертиреоидизъм или други продължителни прояви, а имат ефект само върху симптомите на заболяването.
Преди започване на такова лечение, пациентът трябва да бъде изследван за признаци и симптоми на дехидратация (обезводняване), които често придружават тиреотоксикозата. Бета-блокери не трябва да се прилагат при пациенти с астма.
При пациенти, при които бета-блокерите са противопоказани, могат да се използва калциеви антагонисти (верапамил и дилтиазем).
Лечението с бета-блокери или калциеви антагонисти трябва да се прекрати при нормализиране на функцията на щитовидната жлеза.
— Терапия с антитиреоидни средства:
Антитиреоидни лекарства (например метимазол и пропилтиоурацил) са използвани за лечение на хипертиреоидизъм още от въвеждането им в практиката през 40-те години на миналия век.
Тези препарати се използват за дългосрочен контрол на хипертиреоидизъм при деца, юноши и бременни жени. При възрастни мъже и небременни жени се използват за контрол на хипертиреоидизъм преди провеждане на окончателно лечение.
Антитиреоидните препарати инхибират (потискат) включването на йода в тирозина, тоест потискат синтезата на йодтирозин. Тъй като този процес е необходим за синтезата на щитовидни хормони, производството на щитовидни хормони се потиска, а това води до постепенно намаляване на нивата на щитовидните хормони за 2-8 седмици или повече.
Вторият механизъм на действие на пропилтиоурацил (propylthiouracil), но не и на метимазол (methimazole), е инхибиране превръщането на тироксин (Т4) в трийодтиронин (Т3).Тъй като Т3 е биологични по-активен от Т4, бързото намаляване на нивата на Т3 е свързано с клинично значимо подобрение на симптомите на тиреотоксикоза.
Дозата на антитиреоидния препарат трябва да се коригира на всеки 4 седмици, докато се постигне нормализиране на функцията на щитовидната жлеза.
При някои пациенти с болест на Базедов се наблюдава ремисия след 12-18-месечно лечение, поради което терапията трябва да бъде преустановена. При около половината пациентите в ремисия обаче се наблюдава рецидивиране на хипретиреоидизма след 1 година.
Нодуларните форми на хипертиреоидизъм (тоест токсична полинодозна гуша и токсичен аденом) са с перманентен характер и при тях не се наблюдава ремисия.
Не се препоръчва употребата на метимазол (methimazole) през първия триместър на бременността, тъй като има нисък риск от развитието на пренатални увреждания.
Ако небременна жена, която приема метимазол, планира да забременее, трябва да премине на пропилтиоурацил (propylthiouracil) преди зачеването.
След като достигне до 12 гестационна седмица (седмица на бременността), тя може да се върне към лечение с метимазол, като състоянието й се проследява периодично.
Пропилтиоруацилът се счита за препарат от втора линия при лечението на хипертиреоидизъм.
Той е запазен за употреба при пациенти, които са алергични или нетолерантни към метимазол, както при жени, които са първия триместър на бременността или планират бременност.
Пропилтиоурацилът обаче е лекарство на избор и при състояние на тежка тиреотоксикоза (тиреоидна буря), поради това, че потиска превръщането на Т4 в Т3.
Понижаването на нивата на Т3, който има 20-100 пъти по-голяма биологична активност от Т4, теоретично спомага за по-бързото облекчаване на тиреотоксичните симптоми в сравнение с метимазола.
След като нивата на щитовидните хормони се нормализират, пациентът може да премине към терапия с метимазол.
— Терапия с радиоактивен йод-131 (I 131):
Радиоизотопната терапия с йод-131 (радиоактивен йод) няма толкова бърз ефект както при лечение с антитироидни препарати или тиреоидектомия, но това е ефективен и безопасен метод, който не изисква хоспитализация (престой в болница), като има по-голяма успеваемост от медикаментозното лечение.
Този вид терапия обаче носи по-голям риск за развитие на хипотиреоидизъм при пациенти с болест на Грейвс, което изисква ежедневно лечение с хормонозаместители за цял живот.
Изотопът на радиоактивния йод, използван при тази терапия, е с по-силен ефект от йодните изотопи, използвани за диагностични процедури.
Радиоактивният йод се прилага перорално (през устата) в течна форма или като капсула еднократно. При пациентите, при които не се наблюдава достатъчно силен отговор, понякога се прилага допълнително лечение с радиоактивен йод, но при по-голяма доза.
Йодът се абсорбира бързо и се поглъща от щитовидната жлеза. Нито една друга тъкан или орган в тялото не е в състояние да задържа радиоактивен йод, поради което при тази терапия не се наблюдават много нежелани реакции.
Лечението води до специфичен за щитовидната жлеза възпалителен отговор, който води до фиброза и разрушаване на хиперактивната жлезна тъкан в продължение на няколко седмици до няколко месеца.
Тъй като лечението с радиоактивен йод води до разрушаване на щитовидната тъкан, често след терапията е налице преходен период от няколко дни до няколко седмици, през който симптомите на хипертиреоидизъм могат да се влошат. Това е резултат от освобождаването на хормоните на щитовидната жлеза в кръвта след разрушаването на клетките на щитовидната жлеза, съдържащи хормони.
Прилагането на литий в седмиците след радиоактивната йодна терапия може да удължи задържането на радиоактивен йод в жлезата и така да се повиши неговата ефикасност. Ползите от комбинирането на литий с радиоактивен йод трябва да бъдат преценени спрямо токсичността, свързана с литий.
Терапия с радиоактивен йод никога не трябва да се прилага при бременни жени, тъй като йодът може да премине през плацентата и да засегне щитовидната жлеза на плода, което да доведе до хипотиреоидизъм.
Кърменето също е противопоказно, тъй като радиоизотопът преминава в кърмата.
Ето защо преди започване на терапията с радиоактивен йод се правят изследвания за бременност, като се препоръчва пациентката да не забременява поне 3-6 месеца след лечението или докато не се нормализират функциите на щитовидната жлеза.
Радиоактивен йод обикновено не се прилага при пациенти с тежка офталмопатия, тъй като има данни, че тя се влошава в различна степен след този вид терапия.
Пациентите с леко изразени или никакви офталмологични симптоми могат да намалят рисковете за усложнения чрез едновременното приложение на преднизон в продължение на 6 седмици.
Рискът от офталмопатия е по-висок при пушачи.
— Тироидектомия (оперативно отстраняване на щитовидната жлеза):
Субтоталната тироидектомия (отстраняване на част от жлезата) е най-старият метод за лечение на хипертиреоидизъм.Тотална тироидектомия (премахване на цялата жлеза) и комбинации от хемитиреоидектомия и контралатерална (от срещуположната страна) субтотална тиреоидектомия също са били използвани.
Поради отличната ефикасност на антитиреоидните медикаменти и терапията с радиоактивен йод при регулиране на функцията на щитовидната жлеза, тиреоидектомията не се използва широко, като обикновено се прилага при определени обстоятелства, включително:
- тежък хипертиреоидизъм при деца;
- бременни жени, които не реагират или имат непоносимост към лечението с антитиреоидни средства;
- пациенти с големи по размер щитовидни жлези или тежка офталмопатия;
- пациенти, отказващи радиоактивна терапия с йод;
- пациенти с рефрактерен (неподатлив на лечение) амиодарон-индуциран хипертиреоидизъм;
- пациенти, при които е необходимо бързо нормализиране на функцията на щитовидната жлеза, като например бременни жени, жени, които планират да забременеят през следващите 6 месеца или пациенти с нестабилни сърдечни състояния;
Подготовката за тиреоидектомия включва прилагането на антитиреоидни препарати, стабилен (нерадиоактивен) йод и бета-блокери.
Терапията със стабилен йод намалява отделянето на щитовидни хормони и намалява кръвотока през жлезата, което може да спомогне за намаляване на загубата на кръв по време на операция.
Възможните усложнения при тиреоидектомия включват увреждания на рекурентния ларингеален нерв (nervus laryngeus recurrens), както и отстраняване на паращитовидните жлези.
- Категория: статии
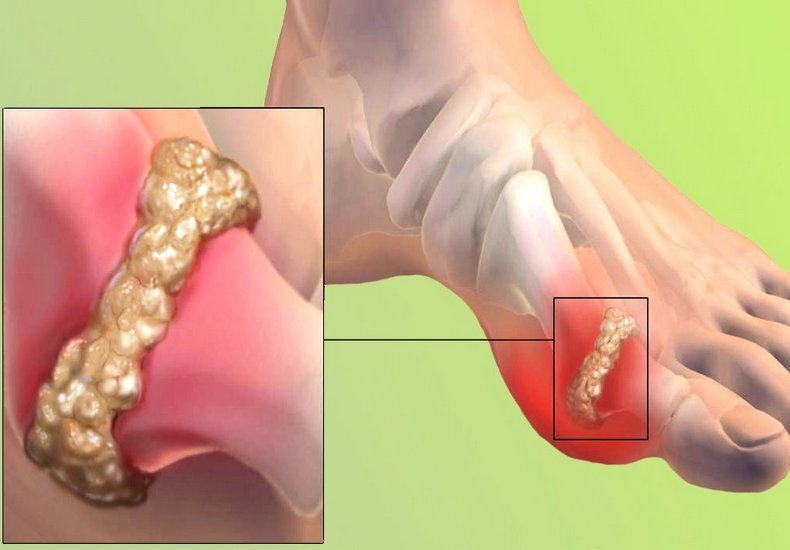
Подагра - описание, причини, симптоми, превенция
Подаграта е медицинско състояние, което обикновено се характеризира с повтарящи се пристъпи на остър възпалителен артрит – зачервена, болезнена, възпалена става. Най-често засегната (при около 50% от случаите) е метатарзофалангеалната става в основата на големия пръст на крака. Тя обаче може да се прояви и под формата на тофуси, камъни в бъбреците или уратна нефропатия. Смята се, че подаграта се причинява от високите нива на пикочна киселина в кръвта, но най-нови изследвания показват, че причината за подаграта е липсата в човешкия организъм на ензима уриказа, което води до кристализация на пикочната киселина, при което кристалите се отлагат в ставите, сухожилията и околните тъкани.
Подаграта е смущение на пуриновия метаболизъм и се проявява когато нейният краен метаболит – пикочната киселина, кристализира под формата на мононатриев урат, който се натрупва в ставите, по сухожилията и заобикалящите ги тъкани. Тези кристали след това предизвикват локална имуноопосредствана възпалителна реакция, като един от ключовите белтъци в каскадата на възпалението е интерлевкин 1β. Загубата на уриказа, която разбива пикочната киселина, в резултат на еволюцията при хората и по-висшите примати, е направила това състояние често срещано.
Подаграта е изключително болезнена болест, която в повечето случаи засяга само една става. Обикновено има два източника на болка - кристалите вътре в ставата, които причиняват болка при движение на засегнатата област, и възпалението на тъканите около ставата, което причинява подуване на кожата и при най-малкия допир също може да се предизвика болка.
Клиничната диагноза се потвърждава чрез наблюдаване на характерните кристали в ставната течност. Лечението с нестероидни противовъзпалителни средства (НСПВС), стероиди или колхицин облекчава симптомите, без да премахва причината, а именно кристалите на пикочната киселина. Те остават между ставните повърхности и продължават да ги износват и дразнят. След като острият пристъп отмине, нивата на пикочна киселина обикновено се понижават чрез промяна в начина на живот.
Симптоми
Кристалите на пикочна киселина могат да се натрупат като твърди, безболезнени натрупвания, известни като тофуси. Причината е липсата в човешкия организъм на ензима уриказа, който превръща водонеразтворимите кристали на пикочната киселина във водоразтворими. Обширните тофуси могат да причинят хроничен артрит в резултат на ерозията на костите. Може да се стигне и до натрупването на кристали, отлагащи се в бъбреците, което води до образуване на камъни в бъбреците и последващата го уратна нефропатия.
Причини
Хиперурикемията не е основната причина за подаграта. Тя може да се появи по редица причини, включително хранителни навици, генетична предразположеност или намалено отделяне на урат солите на пикочната киселина. Основната причина за хиперурикемията е, че организмът има увеличена нужда от антиоксидантна защита, тъй като пикочната киселина при хората осигурява над половината от антиоксидантния капацитет на кръвната плазма. Затова и се увеличава съдържанието на пикочна киселина в кръвта.
Кръвни изследвания
Хиперурикемията не е класическа характерна черта на подаграта, тъй като при почти половината от случаите тя се развива без хиперурикемия, а повечето хора, при които се наблюдават повишени нива на пикочна киселина, никога не развиват подагра. Следователно, диагностичната полза от измерването на нивото на пикочната киселина е относителна. Хиперурикемията се дефинира като нива на урат в плазмата по-големи от 420 μmol/l (7 mg/dl) при мъже и 360 μmol/l (6 mg/dl) при жени. Други често извършвани кръвни изследвания са преброяване на левкоцити, електролити, бъбречна функция и скорост на утайка на еритроцити (СУЕ). Въпреки това както броя на белите кръвни клетки, така и СУЕ могат да бъдат повишени поради подагра и при липса на инфекция. Документирано е преброяване на бели кръвни клетки в количество 40,0×109/l (40,000/mm3).
Превенция
Както промени в начина на живот, така и лекарства могат да понижат нивата на пикочна киселина. Ефективните промени в начина на живот и спазването на диети включват намален прием на такива храни, като месо и морски продукти, прием на достатъчно количество витамин C, който е един от най-силните антиоксиданти и подпомага антиоксидантната защита на организма. Това автоматично намалява съдържанието на пикочна киселина в организма. Ограничаването на консумацията на алкохол и фруктоза и предотвратяването на затлъстяване също оказва положително влияние. Спазването на нискокалорична диета при затлъстели мъже намалява нивата на пикочна киселина със 100 µmol/l (1,7 mg/dl). Ежедневният прием на 1500 mg витамин C намалява риска от развиване на подагра с 45%. Консумацията на кафе, но не и чай, е свързана с нисък риск от развиване на подагра. Подагра може да се развие като вторично заболяване при сънна апнея, поради освобождаването на пурини от страдащите от недостиг на кислород клетки. Лечението на апнея може да намали появата на пристъпи.
Лечение
Основната цел на лечението е овладяване на симптомите на остър пристъп. Превенция на повтарящи се пристъпи не може да се осъществи ефективно чрез прием на различни лекарства за намаляване на серумните нива на пикочна киселина, тъй като при почти половината от случаите подаграта се развива без хиперурикемия, а повечето хора, при които се наблюдават повишени нива на пикочна киселина, никога не развиват подагра. Прилагането на лед за 20 – 30 минути няколко пъти на ден облекчава болката. Възможностите за лечение на остри пристъпи включват нестероидни противовъзпалителни средства (НСПВС), колхицин и стероиди, а за превенция се използват алопуринол, фебуксостат и пробенецид. Намаляването на нивата на пикочна киселина не може да излекува заболяването, а в същото време може да влоши антиоксидантната защита на организма. Лечението на съпътстващи заболявания също е важно.
Алтернативен начин за лечение на подагра са билките, които са доказали своето благотворно въздействие при това заболяване от столетия. Профилактиката на подагра с билки, които са доказали своето благотворно въздействие при това заболяване от столетия, е най-природосъобразният и без странични негативни последствия метод. Те превръщат във водоразтворими кристалите на пикочната киселина, като по този начин премахват причината за подаграта.
Прогноза
Без лечение острият пристъп на подагра обикновено се разсейва за пет до седем дни. 60% от хората, обаче, получават втори пристъп в рамките на една година. Хората с подагра са с повишен риск от високо кръвно налягане, захарен диабет, метаболитен синдром и бъбречно и сърдечно-съдово заболяване.Това може да се дължи отчасти на връзката ѝ с инсулинова резистентност и затлъстяване, но в някои случаи повишеният риск се явява независим.
Без третиране епизодите на остра подагра могат да се развият в хронична подагра с разрушаване на ставните повърхности, деформация на ставите и безболезнени подагрични удебеления на ставите (тофуси). Тези подагрични удебеления на ставите настъпват в 30% от случаите, които не са третирани в продължение на пет години, често пъти в хрущялната извивка на ушната мида, над процесите на олекранона или върху ахилесовите сухожилия. С агресивно третиране те могат да се разтопят. Бъбречните камъни също често усложняват подаграта, като засягат 10 и 40% от хората и настъпват поради ниско рН на урината, което спомага за утаяването на пикочна киселина. Могат да настъпят и други форми на хронична бъбречна дисфункция.
- Категория: статии
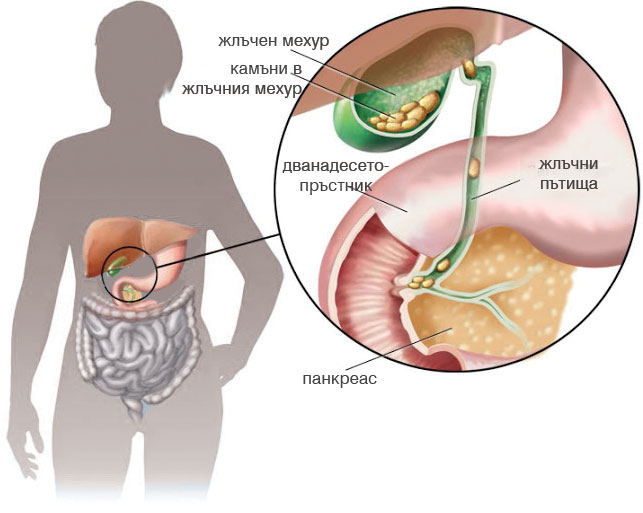
Камъни в жлъчката
Факторите, които определят нормалното функциониране на жлъчния мехур са три - съдържанието на холестерол в кръвта, на микроелементи и на стомашните киселини. Тези проблеми са по-характерни за жените. В САЩ всяка десета жена има жлъчнокаменна болест, в България няма такава статистика, но може би всяка 12-13 жена е засегната от това заболяване без да знае. Мъжките хормони пазят силния пол от образуването на камъни в жлъчния мехур. Но всяка една стресова ситуация може да наруши това фино равновесие, което представлява нашата жлъчка. Тя е един много сложен наситен разтвор, в който вода, киселини, холестерол и микроелементи са в равновесие. Всеки фактор, който наруши равновесието му, може да стане причина за образуването на утайка, а след това на песъчинки, както и да отключи цялата верига за образуване на камъни. Застрашени са хора с високо съдържание на холестерол в кръвта, с наднормено тегло, както и хора, прекарали някои остри вирусни инфекции, тежки дехидратации. Дори за един най-обикновен грип. Той може да предизвика нарушение в електролитния или водния баланс и да доведе до нарушени функции на бъбреците и черния дроб. Дори едно рязко изтощаване на организма или дехидратация може да бъде отключващ момент за образуването на камъни. Бременността също често води до появата на камъни в жлъчката.
Симптоми най-често са болката, дискомфорта след хранене, повръщането. Понякога повръщането е водещо, а болката се появява няколко месеца след това. Но дискомфорта, неудобството, подпирането в дясното подребрие са изключително характерни. Това са малки симптоми, които, ако се търсят целево, ще помогнат да се установи заболяването.
Пожълтяването е много късен симптом. За съжаление тук говорим за така наречената усложнена жлъчнокаменна болест. Установено е, че ако от сто човека 30 са със заболявания на жлъчния мехур, от тях 10 ще имат и патология в големите жлъчни пътища. На практика пожълтяването е израз на запушване на големия жлъчен път, през който преминава жлъчката, за да навлезе в храносмилателната система. Образуването на камъчета и песъчинки, както и на възпалителни процеси довежда до пожълтяване. Това не е хепатит, а пожълтяване следствие на запушване на жлъчните пътища.
Жлъчните камъни са различни по вид в зависимост от образуването си. Най-чести са смесените, но има и холестеролни или пигментни при хората с хематологични заболявания. Освен това никой не знае кога е започнало образуването им.
Камъни консервативно не се лекуват, има симптоматично лечение, което да овладее болката и възпалението, но разрушаването на самите камъни е невъзможно. Така че приемането на различни медикаменти, билки, които уж да доведат до изхвърляне на камъните е невъзможно. Те дори технически е невъзможно да минат през пикочните пътища. Единственият радикален начин на лечение, това е хирургията и отстраняването на жлъчния мехур с камъните, защото той вече не изпълнява своята роля на склад за концентрирана жлъчка. Когато е увреден, той се превръща в малка бомбичка, която е готова да избухне при някаква причина, като хранене с много мазнини или подправки, както и при използването на някои медикаменти.
В момента стандарт за лечение е лапароскопската холецистектомия или отстраняването на жлъчката чрез няколко дупчици в корема на пациента. Разбира се, винаги има малък риск при усложнени форми, когато се налага да се прибегне до отворена хирургия. Но в повечето случаи златният стандарт са лапароскопските операции.
Най-важните предимства на тези интервенции са, че отстранявайки патологичния орган, се дава възможност човека да се възстанови максимално бързо. Защото причината за нетрудоспособност не е отстранения жлъчен мехур, а болката и всички усложнения, които могат да настъпят при една голяма рана на коремната стена. В миналото са се давали по два-три месеца болнични, а сега е напълно възможно на 15-20 ден човек да се върне на работа.
Много рядко се стига до истинско спукване на жлъчния мехур. Защото човек не може да изтърпи болката, за да се стигне дотам. Най-често първо идва възпалението и настъпват тежки страдания, заради които пациентите отиват на лекар. Проблемът е, че когато мехурът е спокоен операцията протича по един начин, а когато е възпален, възможностите за усложнение са повече. Затова нашият съвет винаги е бил още след първата криза пациентите да се насочат към оперативно лечение. За съжаление много малко хора в България го правят заради недоверие към системата.
За да се смали до минимум рискът от появата на камъни в жлъчката хората трябва да внимават с храненето и медикаментите, които приемат. Напоследък има много млади мъже, които се занимават с боди билдинг и приемат хранителни добавки, неразбирайки какво си причиняват в бъдеще. Заради това зачестяват случаите на проблеми в обмяната на веществата. За широкия кръг хора обаче най-важно е храненето и наднорменото тегло. Трябва да се консумира повече растителна храна. Рязкото отслабване също не е добро. За да сте здрави, трябва да се води нормален живот.
Камъни в жлъчката - билкови рецепти
Страница 2 от 6